Пралуент
Склад
діюча речовина: алірокумаб;
1 мл розчину містить алірокумабу 75 мг або 150 мг;
допоміжні речовини: L-гістидин, L-гістидину моногідрохлориду моногідрат, сахароза, полісорбат 20, вода для ін’єкцій.
Лікарська форма
Розчин для ін’єкцій.Основні фізико-хімічні властивості: прозорий розчин, безбарвний або блідо-жовтого кольору.
Фармакотерапевтична група
Ліпідомодифікуючі засоби. Код АТХ С10А Х.Фармакологічні властивості
Механізм дії. Алірокумаб є препаратом повністю людських моноклональних антитіл IgG1, що зв'язуються з високою афінністю та специфічністю з пропротеїновою конвертазою субтилізин-кексинового типу 9 (PCSK9). PCSK9 зв'язується з рецепторами ліпопротеїнів низької щільності (ЛПНЩ) на поверхні гепатоцитів, в результаті чого знижується активність рецепторів ЛПНЩ в печінці. Рецептори ЛПНЩ є головними рецепторами, що відповідають за зниження рівня циркулюючих ЛПНЩ. Таким чином, зниження активності рецепторів ЛПНЩ внаслідок впливу PCSK9 призводить до підвищення рівнів холестерину ЛПНЩ в крові. Шляхом пригнічення зв'язування PCSK9 з рецепторами ЛПНЩ алірокумаб призводить до збільшення кількості рецепторів ЛПНЩ, які здатні взаємодіяти з ЛПНЩ, знижуючи таким чином рівень холестерину ЛПНЩ.
Рецептори ЛПНЩ також зв'язуються з багатими на тригліцериди ліпропротеїнами дуже низької щільності (ЛПДНЩ), залишковими ліпопротеїнами та ліпопротеїнами проміжної щільності (ЛППЩ). Таким чином, лікування алірокумабом може зумовити зниження рівнів цих залишкових ліпопротеїнів, про що свідчить зумовлене ним зниження рівнів аполіпопротеїну В, холестерину неліпопротеїнів високої щільності та тригліцеридів. Алірокумаб також призводить до зниження рівня ліпопротеїну (а), що є формою ЛПНЩ, яка зв'язується з аполіпопротеїном (а). Однак було показано, що рецептори ЛПНЩ мають низьку афінність до ліпопротеїну (а); таким чином, точний механізм, за яким алірокумаб знижує рівень ліпопротеїну (а), залишається не до кінця з'ясованим.
В рамках генетичних досліджень у людей були виявлені варіанти генів PCSK9 з мутаціями, що призводили або до втрати функції, або до посилення функції. Індивіди з мутацією одного алельного гена PCSK9, що призводила до втрати функції, мали нижчі рівні холестерину ЛПНЩ, що корелювало зі значущим зниженням частоти виникнення ішемічної хвороби серця. Було повідомлено про кількох індивідів, у яких відбулись мутації двох алельних генів PCSK9, що призвели до втрати функції, та у яких рівні холестерину ЛПНЩ були надзвичайно низькими при нормальних рівнях холестерину ЛПВЩ та тригліцеридів. І навпаки, мутації гена PCSK9, які призводили до посилення функції, були виявлені в пацієнтів з підвищенням рівнів холестерину ЛПНЩ та з клінічним діагнозом сімейної гіперхолестеринемії.
В рамках багатоцентрового, подвійного сліпого плацебо-контрольованого 14-тижневого дослідження 13 пацієнтів з гетерозиготною сімейною гіперхолестеринемією, зумовленою мутаціями гена PCSK9, які призвели до посилення функції, були рандомізовані в групи, які отримували або алірокумаб в дозі 150 мг кожні 2 тижні, або плацебо. Середній вихідний рівень холестерину ЛПНЩ становив 151,5 мг/дл (3,90 ммоль/л). На тижні 2 середнє зниження рівня холестерину ЛПНЩ порівняно з вихідним рівнем становило 62,5% у групі пацієнтів, що отримували алірокумаб, проти 8,8% у групі пацієнтів, що отримували плацебо. На тижні 8 середнє зниження рівня холестерину ЛПНЩ порівняно з вихідним рівнем у всіх пацієнтів, що отримували алірокумаб, становило 72,4%.
Фармакодинаміка.
В дослідженнях в умовах in vitro алірокумаб не спричинював Fc-опосередковану ефекторну функціональну активність (антитілозалежну клітиноопосередковану токсичність та комплементзалежну цитотоксичність) як при наявності, так і при відсутності PCSK9; крім цього, при зв'язуванні алірокумабу з PCSK9 не спостерігалось утворення ніяких розчинних імунних комплексів, здатних до зв'язування білків системи комплементу.
Педіатрична популяція. Європейське агентство лікарських засобів звільнило виробника від зобов'язання надати результати досліджень з вивчення застосування препарату Пралуент для лікування підвищеного рівня холестерину в одній чи в кількох підгрупах педіатричної популяції (інформація щодо застосування препарату дітям наведена в розділі «Спосіб застосування та дози»).
Європейське агентство лікарських засобів звільнило виробника від зобов'язання надати результати досліджень з вивчення застосування препарату Пралуент для лікування змішаної дисліпідемії в усіх підгрупах педіатричної популяції (інформація щодо застосування препарату дітям наведена в розділі «Спосіб застосування та дози»).
Фармакокінетика.
Абсорбція. Після підшкірного введення алірокумабу в дозі від 50 до 300 мг медіана часу до досягнення максимальної концентрації в сироватці крові (tmax) становила 3-7 днів. Фармакокінетичні показники алірокумабу після однократного підшкірного введення в дозі 75 мг в ділянку живота, плеча та стегна були подібними. Абсолютна біодоступність алірокумабу після підшкірного введення становила приблизно 85% згідно з результатами популяційного фармакокінетичного аналізу. Рівноважна концентрація досягалась після введення 2-3 доз з приблизно 2-кратним коефіцієнтом кумуляції.
Розподіл. Після внутрішньовенного введення об'єм розподілу становив приблизно від 0,04 до 0,05 л/кг, що вказує на те, що розподіл алірокумабу здійснюється головним чином через систему кровообігу.
Біотрансформація. Спеціальні дослідження метаболізму не проводились, оскільки алірокумаб є білком. Передбачається, що алірокумаб розщеплюється до низькомолекулярних пептидів та окремих амінокислот.
Виведення. Виявлено два шляхи виведення алірокумабу. При низьких концентраціях виведення препарату переважно здійснюється через насичуване зв'язування з мішенню (PCSK9), а при вищих концентраціях виведення алірокумабу здійснюється головним чином ненасичуваним протеолітичним шляхом.
Згідно з результатами популяційного фармакокінетичного аналізу медіана уявного періоду напіввиведення алірокумабу при рівноважних концентраціях знаходилась в межах від 17 до 20 днів у пацієнтів, які отримували алірокумаб як монотерапію шляхом підшкірного введення в дозі або 75 мг кожні 2 тижні, або 150 мг кожні 2 тижні. При одночасному застосуванні зі статином медіана уявного періоду напіввиведення алірокумабу становила 12 днів.
Лінійність/нелінійність. При 2-кратному збільшенні дози з 75 мг до 150 мг кожні 2 тижні спостерігалось дещо більше, ніж дозопропорційне, збільшення загальної концентрації алірокумабу (2,1-2,7-кратне збільшення).
Особливі популяції пацієнтів.
Пацієнти літнього віку. Згідно з результатами аналізу фармакокінетичних показників кореляція віку пацієнта з експозицією алірокумабу при рівноважних концентраціях була незначною, без впливу на ефективність чи безпеку препарату.
Стать. Згідно з результатами популяційного фармакокінетичного аналізу стать пацієнта не впливала на фармакокінетичні показники алірокумабу.
Расова приналежність. Згідно з результатами популяційного фармакокінетичного аналізу расова приналежність не впливала на фармакокінетичні показники алірокумабу. Після однократного підшкірного введення алірокумабу в дозі від 100 мг до 300 мг значущої відмінності між його експозиціями у здорових добровольців японської національності та представників європеоїдної раси не було.
Маса тіла. Маса тіла була визначена в остаточній популяційній фармакокінетичній моделі як одна значуща коваріата, що впливає на фармакокінетичні показники алірокумабу. Експозиція алірокумабу (AUC0-14d) при рівноважних концентраціях при обох схемах дозування (75 та 150 мг кожні 2 тижні) була знижена на 29 % та 36 % у пацієнтів з масою тіла понад 100 кг у порівнянні з пацієнтами з масою тіла в межах від 50 кг до 100 кг. Проте це не обумовлювало клінічно значущих відмінностей в зниженні рівнів холестерину ЛПНЩ.
Порушення функції печінки. В дослідженні І фази після однократного підшкірного введення в дозі 75 мг фармакокінетичні профілі алірокумабу у пацієнтів з легким та помірним порушенням функції печінки були подібними до фармакокінетичних профілів у осіб з нормальною функцією печінки. Даних щодо застосування препарату пацієнтам з тяжким порушенням функції печінки немає.
Порушення функції нирок. Оскільки немає даних щодо того, що моноклональні антитіла виводяться нирками, вважається, що функція нирок не впливає на фармакокінетичні показники алірокумабу. Результати популяційних фармакокінетичних аналізів показали, що експозиція алірокумабу (AUC0-14d) при рівноважних концентраціях при обох схемах дозування (75 та 150 мг кожні 2 тижні) була збільшена на 22-35 % та 49-50 % у пацієнтів з легким та помірним порушенням функції нирок відповідно у порівнянні з особами з нормальною функцією нирок. Найбільш ймовірною причиною відмінностей у фармакокінетичних показниках є різний розподіл показників маси тіла та віку – двох коваріат, які впливають на експозицію алірокумабу, – у пацієнтів, що належали до різних категорій за функцією нирок. Дані щодо застосування препарату пацієнтам з тяжким порушенням функції нирок є обмеженими; у таких пацієнтів експозиція алірокумабу була приблизно у 2 рази вищою у порівнянні з особами з нормальною функцією нирок.
Зв’язок між фармакокінетикою та фармакодинамікою. Фармакодинамічний ефект алірокумабу щодо зниження рівня холестерину ЛПНЩ є непрямим та опосередкований через зв'язування з PCSK9. До досягнення цільового насичення спостерігається залежне від концентрації зниження вільної PCSK9 та холестерину ЛПНЩ. Після насичуваного зв'язування PCSK9 подальше збільшення концентрацій алірокумабу не призводить до подальшого зниження рівня холестерину ЛПНЩ, проте при цьому спостерігається подовження ефекту зниження рівня холестерину ЛПНЩ.
Доклінічні дані з безпеки. Доклінічні дані свідчать про відсутність особливої небезпеки для людини, що підтверджується результатами оцінки фармакологічної безпеки та токсичності при застосуванні багатократних доз препарату.
Дослідження токсичного впливу на репродуктивну систему у тварин показали, що алірокумаб, подібно до інших антитіл IgG, проникає через плацентарний бар’єр.
Побічних ефектів на сурогатні маркери фертильності (таких як естральний цикл, об’єм яєчок, об’єм еякуляту, рухливість сперматозоїдів або загальна кількість сперматозоїдів в еякуляті) у тварин виявлено не було; в жодному дослідженні токсичного впливу у тварин не було виявлено також пов’язаних з алірокумабом патоанатомічних чи гістопатологічних змін тканин репродуктивної системи.
У тварин побічних впливів на ріст чи розвиток плода виявлено не було. Токсичного впливу на материнський організм у вагітних самок мавп не було виявлено при системній експозиції, що у 81 раз перевищувала експозицію в людини при застосуванні препарату в дозі 150 мг кожні 2 тижні. Однак токсичний вплив на материнський організм спостерігався у вагітних самок щурів при системній експозиції, що в перерахунку приблизно в 5,3 раза перевищувала експозицію в людини при застосуванні препарату в дозі 150 мг кожні 2 тижні (для перерахунку була використана експозиція, виміряна в невагітних самок тварин впродовж 5-тижневого дослідження токсичного впливу).
У потомства тварин, що зазнавало впливу високих доз алірокумабу щотижня впродовж усього періоду вагітності, відзначалась більш слабка вторинна імунна відповідь на антигенну стимуляцію, ніж у потомства тварин контролю. Жодних інших доказових даних щодо імунної дисфункції у потомства, пов'язаної з алірокумабом, немає.
Клінічні характеристики
Показання
Пралуент застосовують дорослим пацієнтам з первинною гіперхолестеринемією (гетерозиготною сімейною та несімейною) або змішаною дисліпідемією як додаткову терапію до дієти:
- у комбінації зі статином або зі статином та іншими ліпідознижуючими засобами, якщо цільовий рівень холестерину ЛПНЩ не досягається при застосуванні максимальної переносимої дози статину;
- у вигляді монотерапії чи в комбінації з іншими ліпідознижуючими засобами у разі непереносимості статинів або коли застосування статинів протипоказане.
Протипоказання
Гіперчутливість до діючої речовини або до будь-якої з допоміжних речовин (див. розділ «Склад»). Період вагітності та годування груддю. Дитячий вік до 18 років.
Взаємодія з іншими лікарськими засобами та інші види взаємодій
Вплив алірокумабу на інші лікарські засоби. Оскільки алірокумаб є біологічним лікарським засобом, жодного фармакокінетичного впливу алірокумабу на інші лікарські засоби та жодного впливу на ферменти цитохрому Р450 не очікується.
Вплив інших лікарських засобів на алірокумаб. Відомо, що статини та інші засоби, які впливають на рівень ліпідів, збільшують продукування білка PCSK9 (пропротеїнова конвертаза субтилізин-кексинового типу 9), що є мішенню для алірокумабу. Це призводить до збільшення мішень-опосередкованого кліренсу та зниження системної експозиції алірокумабу. У порівнянні з монотерапією алірокумабом при одночасному застосуванні зі статинами, езетимібом та фенофібратом експозиція алірокумабу є нижчою приблизно на 40 %, 15 % та 35 % відповідно. Однак зниження рівня холестерину ЛПНЩ підтримується впродовж періоду між введеннями алірокумабу при його застосуванні кожні два тижні.
Особливості застосування
Алергічні реакції. В рамках клінічних досліджень повідомлялось про загальні алергічні реакції, включаючи свербіж, а також про такі рідкісні та інколи серйозні алергічні реакції, як гіперчутливість, нумулярна екзема, кропив’янка та алергічний васкуліт (див. розділ «Побічні реакції»). У разі виникнення серйозних алергічних реакцій потрібно припинити застосування препарату Пралуент та розпочати відповідне симптоматичне лікування (див. розділ «Протипоказання»).
Порушення функції нирок. У клінічних дослідженнях була представлена обмежена кількість пацієнтів з тяжким порушенням функції нирок (що визначалось, коли розрахована ШКФ становила 2) (див. розділ «Фармакокінетика»). Пралуент потрібно застосовувати з обережністю пацієнтам з тяжким порушенням функції нирок.
Порушення функції печінки. Застосування препарату пацієнтам з тяжким порушенням функції печінки (клас С за класифікацією Чайлда-П'ю) не вивчалось (див. розділ «Фармакокінетика»). Пралуент потрібно застосовувати з обережністю пацієнтам з тяжким порушенням функції печінки.
Застосування у період вагітності або годування груддю.
Вагітність. Даних щодо застосування препарату Пралуент вагітним жінкам немає. Алірокумаб є препаратом рекомбінантних антитіл IgG1, у зв’язку з чим передбачається, що він проходить через плацентарний бар’єр. Застосування препарату Пралуент під час вагітності протипоказано.
Годування груддю. Невідомо, чи алірокумаб проникає у грудне молоко людини. Людський імуноглобулін G (IgG) екскретується в грудне молоко, особливо в молозиво, застосування препарату Пралуент протипоказано жінкам, які годують груддю. Оскільки вплив алірокумабу на немовлят, що вигодовуються грудним молоком, невідомий, потрібно прийняти рішення щодо припинення годування груддю або припинення застосування препарату Пралуент впродовж цього періоду.
Фертильність. Даних щодо побічних впливів на фертильність людини немає.
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами.
Вплив препарату Пралуент на здатність керувати транспортними засобами та працювати з іншими механізмами відсутній або незначний.
Спосіб застосування та дози.
Дозування. Перед початком застосування препарату Пралуент потрібно виключити вторинні причини гіперліпідемії або змішаної дисліпідемії (наприклад нефротичний синдром, гіпотиреоз).
Звичайна початкова доза препарату Пралуент становить 75 мг, що вводиться підшкірно один раз кожні 2 тижні. Для пацієнтів, яким необхідне більш значне зниження холестерину ЛПНЩ (> 60 %), початкова доза препарату може становити 150 мг, що вводиться підшкірно один раз кожні 2 тижні.
Доза препарату Пралуент може бути підібрана індивідуально, з урахуванням таких параметрів пацієнта, як вихідний рівень холестерину ЛПНЩ, мета терапії та відповідь на лікування. Оцінку рівнів ліпідів можна провести через 4 тижні після початку лікування препаратом або титрування його дози, коли, як правило, досягаються рівноважні концентрації холестерину ЛПНЩ, та відповідно до результатів відкоригувати дозу препарату (провести титрування з підвищенням або зі зменшенням дози). Пацієнти повинні отримувати найнижчу дозу препарату, яка необхідна для досягнення бажаного зниження рівнів холестерину ЛПНЩ.
Якщо введення дози препарату було пропущено, ін’єкцію потрібно зробити якнайшвидше, після чого наступну дозу препарату слід вводити через два тижні від дати останньої ін’єкції.
Особливі популяції пацієнтів.
Педіатрична популяція. Безпека та ефективність препарату Пралуент для дітей та підлітків (віком до 18 років) не встановлені. Дані з цього приводу відсутні.
Пацієнти літнього віку. Корекція дозування при застосуванні препарату пацієнтам літнього віку не потрібна.
Порушення функції печінки. Пацієнтам з легким чи помірним порушенням функції печінки корекція дозування препарату не вимагається. Даних щодо застосування препарату в пацієнтів з тяжким порушенням функції печінки немає.
Порушення функції нирок. Пацієнтам з легким чи помірним порушенням функції нирок корекція дозування препарату не потрібна. Дані щодо застосування препарату пацієнтам з тяжким порушенням функції нирок обмежені (див. розділ «Фармакокінетика»).
Маса тіла. Корекція дозування препарату залежно від маси тіла пацієнта не потрібна.
Спосіб застосування. Препарат призначений для підшкірного введення.
Пралуент вводиться у вигляді підшкірної ін’єкції в ділянку стегна, живота або плеча.
Рекомендується змінювати місце ін’єкції при кожному наступному введенні препарату.
Ін’єкцію препарату Пралуент не слід здійснювати в ділянки активного захворювання чи ураження шкіри, такого як сонячні опіки, шкірні висипання, запальні процеси або шкірні інфекції.
Пралуент не слід вводити одночасно з іншими ін’єкційними лікарськими засобами в одне місце для введення.
Ін’єкцію препарату Пралуент може здійснювати або сам пацієнт, або особа, що доглядає за пацієнтом, після надання медичним працівником інструкції щодо правильної техніки проведення підшкірної ін’єкції.
Запобіжні заходи перед застосуванням препарату.Перед застосуванням препарат Пралуент потрібно нагріти до кімнатної температури, після чого слід якнайшвидше зробити ін’єкцію.
Попередньо наповнена шприц-ручка чи попередньо наповнений шприц призначені тільки для одноразового застосування.
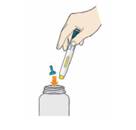
Інструкція щодо використання
попередньо наповненого шприца, який містить 75 мг алірокумабу
На рисунку нижче показано складові частини шприца з препаратом Пралуент.
Діти
Досвіду застосування препарату для лікування дітей немає.Передозування
У контрольованих клінічних дослідженнях не було виявлено ніяких проблем щодо безпеки при більш частому введенні препарату, ніж коли він вводиться згідно з рекомендованим графіком кожні 2 тижні. Специфічної терапії при передозуванні препаратом Пралуент немає. У разі передозування слід провести симптоматичну терапію та за необхідності підтримуючі заходи.
Побічні реакції.
Загальний огляд профілю безпеки препарату. Найбільш частими побічними реакціями були реакції в місці введення препарату, симптоми з боку верхніх відділів дихальних шляхів та свербіж. Найбільш частими побічними реакціями, що призводили до припинення лікування препаратом Пралуент, були реакції в місці введення препарату.
Відмінностей в профілі безпеки препарату при двох схемах дозування (75 мг та 150 мг), що застосовувались в дослідженнях ІІІ фази, виявлено не було.
Побічні реакції представлені за категоріями «Система-Орган-Клас». Частота їхнього виникнення класифікована таким чином: дуже часто (≥ 1/10); часто (≥ 1/100 до
Побічні реакції, про які повідомлялося у пацієнтів, які отримували лікування алірокумабом, за сукупними даними контрольованих досліджень
| Категорії «Система-Орган-Клас» | Часто | Рідко |
| З боку імунної системи | Гіперчутливість, алергічний васкуліт | |
| З боку дихальної системи, органів грудної клітки та середостіння | Ознаки і симптоми з боку верхніх відділів дихальних шляхів* | |
| З боку шкіри та підшкірної клітковини | Свербіж | Кропив’янка, нумулярна екзема |
| Загальні розлади та реакції у місці введення препарату | Реакції в місці ін’єкції** |
* Включаючи головним чином біль у ротоглотці, ринорею, чхання.
** Включаючи еритему/почервоніння, свербіж, припухлість, біль/чутливість
Опис окремих побічних реакцій
Реакції в місці ін’єкції. Про реакції в місці ін’єкції, включаючи еритему/почервоніння, свербіж, припухлість та біль/чутливість, повідомлялося у 6,1 % пацієнтів, які отримували лікування алірокумабом, у порівнянні з 4,1 % пацієнтів контрольної групи (отримували ін’єкції плацебо). Більшість реакцій в місці ін’єкції були транзиторними та легкого ступеня. Частка пацієнтів, що припинили лікування препаратом через місцеві реакції в місці ін’єкції, була порівнянною у двох групах (0,2 % в групі алірокумабу та 0,3 % в контрольній групі).
Загальні алергічні реакції. Про загальні алергічні реакції повідомлялось більш часто в групі алірокумабу (8,1 % пацієнтів), ніж у контрольній групі (7,0 % пацієнтів), головним чином за рахунок різної частоти виникнення свербежу. Випадки свербежу, які спостерігались при цьому, були, як правило, легкого ступеня та короткочасними. Крім цього, в контрольованих клінічних дослідженнях повідомлялось про такі рідкісні та інколи серйозні алергічні реакції, як гіперчутливість, нумулярна екзема, кропив’янка та алергічний васкуліт (див. розділ «Особливості застосування»).
Особливі популяції пацієнтів
Пацієнти літнього віку. Незважаючи на те, що проблем щодо безпеки у пацієнтів віком понад 75 років не спостерігалось, дані про застосування препарату у цій вікові групі є обмеженими. У контрольованих дослідженнях 1158 пацієнтів (34,7 %), що отримували лікування препаратом Пралуент, були віком 65 років та більше, а 241 пацієнт (7,2 %), що отримували лікування препаратом Пралуент, були віком 75 років та більше. Зі зростанням віку значущої відмінності у безпеки та ефективності препарату відзначено не було.
Рівні холестерину ЛПНЩ За сукупними даними контрольованих досліджень у 796 з 3340 пацієнтів (23,8 %), що отримували лікування препаратом Пралуент, значення холестерину ЛПНЩ під час двох послідовних визначень становило
Імуногенність / антитіла до препарату. У дослідженнях ІІІ фази у 4,8 % пацієнтів, які отримували алірокумаб, спостерігалась відповідь на лікування у вигляді появи антитіл до препарату у порівнянні з 0,6 % пацієнтів контрольної групи (які отримували плацебо або езетиміб). У більшості цих пацієнтів було виявлено низькі титри антитіл до препарату без нейтралізуючої активності. У порівнянні з пацієнтами, в яких антитіла до препарату не виявлялись, у пацієнтів з наявністю антитіл до препарату експозиція, ефективність чи безпека алірокумабу жодним чином не відрізнялись, за винятком більшої частоти реакцій в місці ін’єкції препарату. Тільки у 1,2 % пацієнтів були виявлені антитіла з нейтралізуючою активністю, всі ці пацієнти були з групи, що отримувала алірокумаб. У більшості цих пацієнтів тест на антитіла з нейтралізуючою активністю був позитивним тільки в одному зразку. І тільки у 10 пацієнтів (0,3 %) тест на антитіла з нейтралізуючою активністю був позитивним у двох або більше зразках. Наявні дані не свідчать про кореляцію між наявністю антитіл з нейтралізуючою активністю та ефективністю зниження рівня холестерину ЛПНЩ чи безпечністю. Дані щодо імуногенності значною мірою залежать від чутливості та специфічності методу кількісного визначення антитіл до препарату.
Повідомлення про підозрювані небажані реакції. Повідомлення про підозрювані небажані реакції після реєстрації лікарського засобу є важливою процедурою. Це дає змогу продовжувати моніторинг співвідношення ризик/користь для даного лікарського засобу. Медичних працівників просять повідомляти про усі підозрювані небажані реакції через національну систему повідомлень.
Термін придатності
2 роки.Умови зберігання
Зберігати у недоступному для дітей місці. Зберігати в холодильнику (2 - 8 °C). Не заморожувати. Час знаходження препарату не в холодильнику не повинен перевищувати максимум 24 години при температурі нижче 25 °C. Шприц-ручку або шприц зберігати в зовнішній картонній упаковці з метою захисту від світла.
Несумісність
З огляду на відсутність досліджень сумісності цей лікарський засіб не слід змішувати з іншими лікарськими засобами.
Упаковка
По 1 мл упопередньо наповненому шприцу; по 1 або 2 шприца в картонній коробці;по 1 мл у попередньо наповненій шприц-ручці; по 1 або 2 шприц-ручці в картонній коробці.
Категорія відпуску
За рецептом.Виробник
САНОФІ ВІНТРОП ІНДАСТРІА.
Санофі-Авентіс Дойчланд ГмбХ.Місцезнаходження виробника та його адреса місця провадження діяльності
1051 Бульвар Ендустрієль 76580 ЛЬО ТРЕ, Франція.
Індустріпарк Хьохст-Брюнінгштрассе 50 H500, H590, Н600 65926 Франкфурт-на-Майні, Німеччина.




